Des cristaux comestibles

Illustration G. Mühlebach EPFL SPS 2020
Des maths, de la physique, de la chimie et…du sucre comme ingrédients d’un magnifique cristal !
Tu n’as pas envie de creuser sous Terre, ni de casser des tonnes de rochers avant de trouver un cristal ? Voilà une recette qui te permettra, avec bien sûr un peu de patience, de fabriquer ton propre cristal, et pourquoi pas, même de le déguster !
Pour cette expérience, il te faudra :
- 400 g de sucre
- 200 ml d’eau
- 1 pic à brochette
- 1 pincette
- Un verre haut
- Du colorant alimentaire (optionnel)
- Du film plastique (optionnel)
- Et surtout…de la patience !
Pour commencer, mets un peu de sucre dans une assiette, et humidifie ton pic à brochette en le trempant dans un verre d’eau. Roule-le dans le sucre pour que les grains se collent tout autour. Ensuite, laisse sécher un moment.

Pendant ce temps, tu vas préparer un sirop. Pour cela, verse 200 ml d’eau dans une casserole et ajoutes-y 400 g de sucre. Fais bouillir le tout pour que le sucre soit entièrement dissout.
Quand tout le sucre a disparu, tu peux ajouter du colorant alimentaire dans le sirop, pour qu’il prenne une belle couleur. Laisse bien refroidir le sirop avant de le transvaser dans le verre.
Plonge ton pic à brochette enrobé de sucre dans le verre et fais-le tenir en équilibre grâce à une pincette. Ajuste-le pour qu’il ne touche ni le fond du verre ni ses parois. Pour éviter que des saletés tombent dans ton sirop, tu peux mettre du film plastique en haut du verre.
Il ne reste plus qu’à patienter ! Surtout, ne bouge pas ton verre, car ça peut freiner la formation des cristaux. Regarde chaque jour l’évolution de la formation de tes cristaux de sucre. Leur formation peut prendre 1 à 2 semaines, mais tu peux aussi le laisser plus longtemps !
Tu peux aussi regarder cette vidéo :
Mais d’ailleurs, pourquoi est-ce que des cristaux se forment sur ton pic à brochette ? Et prennent-ils des formes particulières ? Auraient-ils la même forme si tu avais utilisé du sel plutôt que du sucre ?
Vérifie ton raisonnement avec les explications ci-dessous :
 |
 |
Comment se forment tes cristaux de sucre ?
Dans la préparation de cette expérience, 2 étapes ont été particulièrement importantes pour que tes cristaux naissent et grandissent. Tu as fait bouillir l’eau avec le sucre et tu as aussi trempé le pic à brochette dans le sucre. Mais comment est-ce que ceci a pu nous aider ?
Occupons-nous tout d’abord de la préparation du sirop. Quand tu as mélangé les 200 ml d’eau avec les 400 g de sucre, tu t’es peut-être aperçu que le sucre ne disparaissait pas complètement, même en le mélangeant avec une cuillère. En effet, avec ces quantités, on se trouve juste à la limite de la saturation. C’est-à-dire qu’à température ambiante (celle de la pièce est d’environ 20°C), 200 ml d’eau ne peut dissoudre qu’environ 400 g de sucre. Mais lorsque le mélange a commencé à chauffer, alors d’un coup, le sucre qui ne s’était pas dissout à disparu. C’est parce que dans 200 ml d’eau en ébullition, on peut dissoudre presque 960 g de sucre !!
Et comme l’eau qui bout s’évapore, on se retrouve avec un sirop qui contient bien 400 g de sucre et moins de 200 ml d’eau. Quand l’eau va refroidir, le sucre qui était dissout va précipiter (redevenir solide) et on aura obtenu une solution qu’on appelle sursaturée en sucre.
Pour que des cristaux se forment, ils doivent se déposer quelque part, sur une aspérité ou une « impureté » de surface. Si nous ne mettions pas le pic à brochette sucré dans le verre, des cristaux se formeraient tout de même, mais sur le bord du verre, qui, malgré son apparence lisse, ne l’est pas au niveau microscopique. La germination (naissance) des cristaux serait également plus lente.
Notre pic à brochette sucré sert donc de plateforme d’accroche aux grains de sucre qui précipitent dans l’eau. Ceux-ci vont s’attacher les uns aux autres pour ne plus être de simples grains de sucres mais former ensemble un réseau de cristaux !
Mais pourquoi les cristaux de sucre ou de sel ont-ils des formes différentes ?
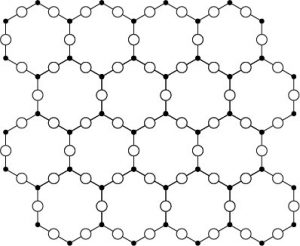
Toute matière est composée d’atomes ou molécules qui vont s’assembler de façon spécifique en se liant entre eux. Quand ils s’assemblent de façon régulière, on peut observer l’apparition d’un motif qui se répète, comme par exemple ci-dessous un motif en nid d’abeilles. C’est cette structure régulière qui va donner naissance à un cristal.
 |
 |
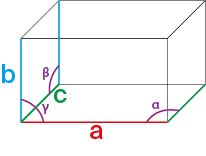
Le motif répété est appelé la maille cristalline élémentaire. Cette maille peut être représentée par une boîte dans laquelle se trouvera la molécule qui se répète. La longueur des côtés a, b et c de cette boîte, ainsi que les angles α, β et γ vont dépendre de la molécule qui se trouve à l’intérieur.
 |
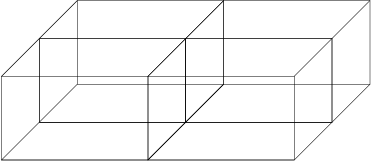
D’autres mailles vont s’attacher à la première pour former un réseau cristallin :
 |
Comme les tailles des côtés ainsi que les angles varient selon la molécule, la forme du cristal sera différente s’il s’agit d’un cristal de sel ou d’un cristal de sucre !
En cliquant sur ce lien, tu trouveras quelques formes possibles de cristaux, selon la forme de leur maille élémentaire. Ci-dessous, tu peux voir des photos de cristaux de sel, de sucre et de ferricyanure, qui sont bien différents !
 |
 |
 |
Cristaux de sel (gauche), de sucre (centre) et de ferricyanure de potassium (droite).
Filme ou photographie, toi aussi, ton expérience et partage nous ton résultat sur les réseaux sociaux :
@EPFL_SPS
Si tu n’as pas accès à ces réseaux sociaux, tu peux toujours nous envoyer ta vidéo par mail, elle sera peut-être publiée sur nos réseaux !

Page d’accueil : Les sciences à la maison
Durant la période d’arrêt de fréquentation des lieux de formation, le Service de promotion des sciences de l’EPFL propose aux curieuses et curieux de tout âge, des activités scientifiques et techniques à faire à la maison.


